
临床组织是分子机制研究的首选样本,但COVID-19临床组织很少,且大多来自终末期患者的尸检。动物模型,尤其是非人灵长类动物模型的建立,可为COVID-19相关研究奠定基础。
2022年1月北京协和医学院杨俊涛教授在Signal transduction and targeted therapy(IF 18.187)杂志上发表题目为“Proteomic and phosphoproteomic profiling of COVID-19-associated lung and liver injury: a report based on rhesus macaques”的研究成果,利用蛋白组学和磷酸化蛋白组学首次对感染SARS-CoV-2的恒河猴早期肺组织和肝组织分子变化进行研究,为进一步研究SARS-CoV-2的分子机制和药物发现提供了有效的数据资源。

研究材料:
空白对照组和病毒感染组;SARS-CoV-2感染7天后的恒河猴肺、肝组织(n=8)
技术路线:
步骤1:肺、肝损伤表型分析
步骤2:蛋白组学分析
步骤3:差异蛋白PPI互作
步骤4:磷酸化蛋白组学分析
步骤5:激酶预测
步骤6:激酶与药物整合预测
研究结果:
1. 恒河猴SARS-CoV-2感染后肺、肝损伤检测
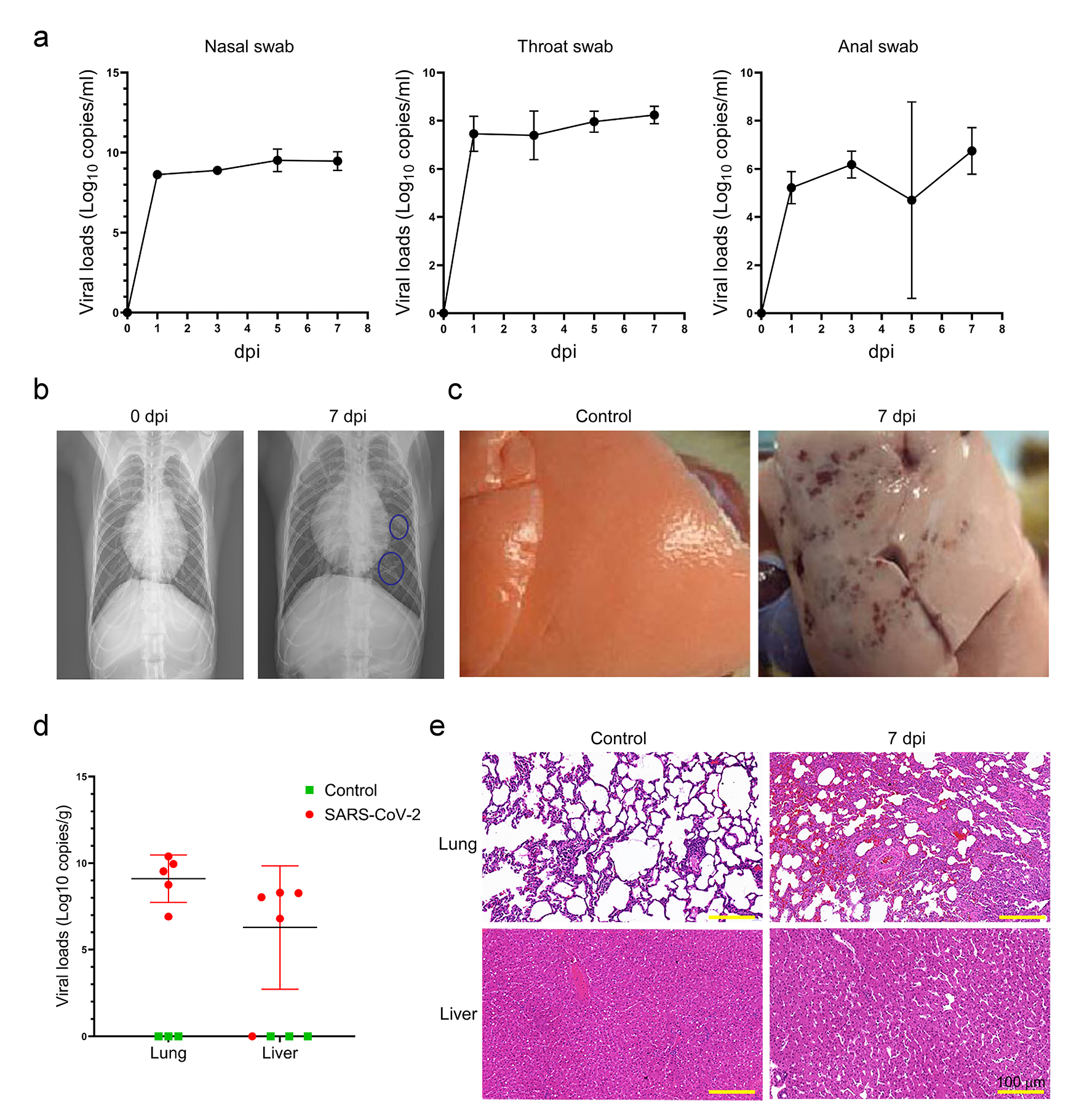
采用定量RT-PCR方法检测感染恒河猴鼻、喉、肛门拭子中SARS-CoV-2 RNA含量,确定7天后SARS-CoV-2 病毒含量趋于稳定(图1a)。从胸片可直观看到,病毒感染组恒河猴肺部间质滤过和渗出性病变(图1b)。与对照组相比,感染组恒河猴肺部有多个病理病变和出血点(图1c)。进一步定量RT-PCR检测发现,感染组恒河猴肝脏中的病毒载量低于肺部(图1d)。从病理切片可以看到感染组恒河猴肺部有明显的炎性细胞浸润,肺间隔局部增厚,血管血栓形成;肝脏中肝窦间隙增宽、炎症细胞散在浸润(图1e)。
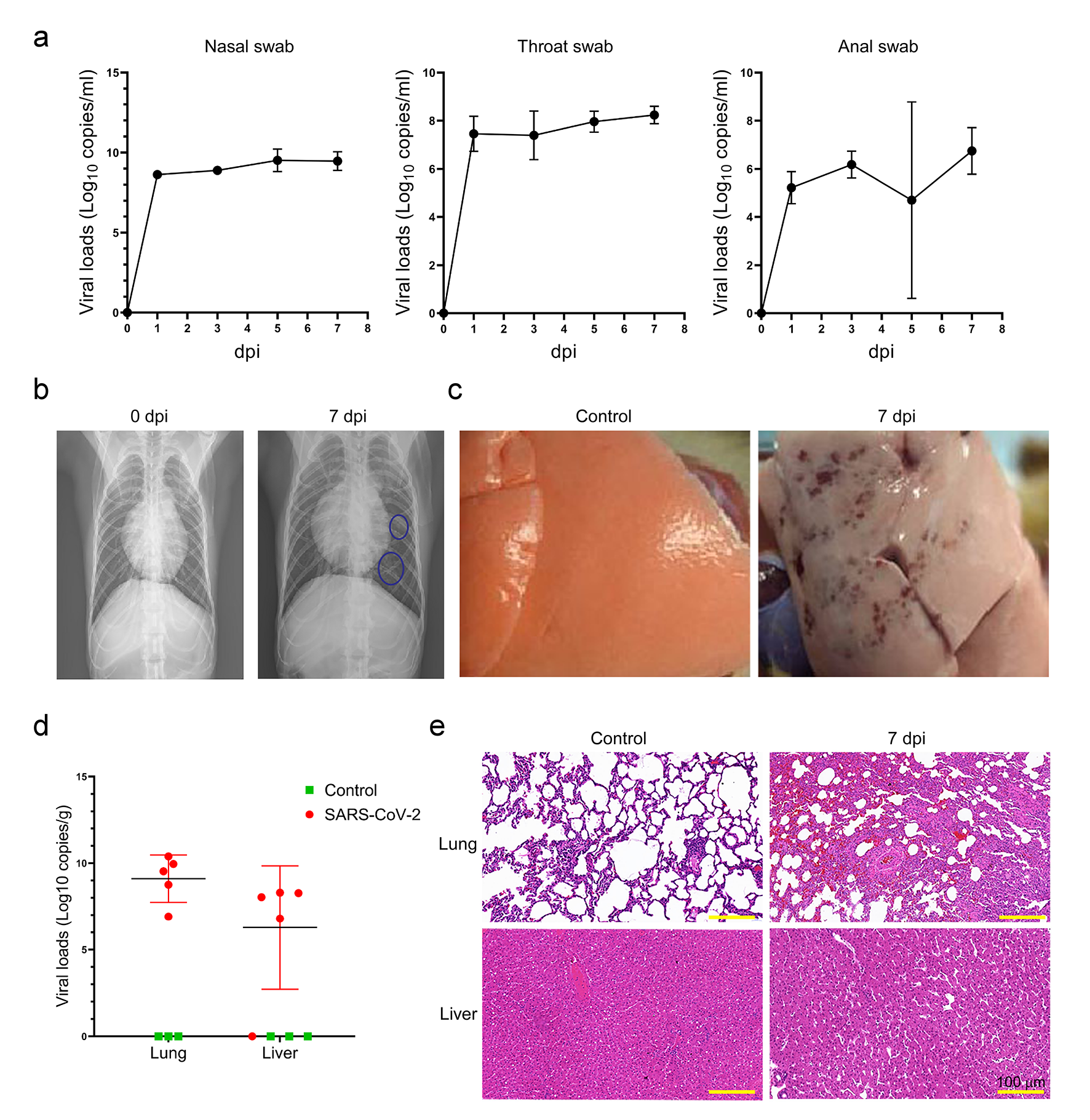
2.恒河猴SARS-CoV-2感染后肺、肝组织蛋白组学分析
蛋白质组学定量了肺中6715个蛋白和肝脏中5238个蛋白。主成分分析(PCA)结果显示,对照组和病毒感染组之间肝脏蛋白表达谱的总体差异大于肺(图2b,c)。与对照组相比,感染组肺组织和肝组织差异表达蛋白分别为757个和1219个(图2d)。KEGG通路富集分析显示,在感染组的肺组织中,核糖体、DNA复制、RIG- I样受体或信号通路、错配修复等相关通路蛋白上调;与ECM -受体相互作用关系最为密切蛋白的下调(图2e)。在感染组的肝脏组织中,核糖体、氨基酰基-tRNA生物合成、氧化磷酸化等相关通路蛋白上调;剪接体、调控肌动蛋白细胞骨架和局部粘附等相关蛋白下调(图2f)。
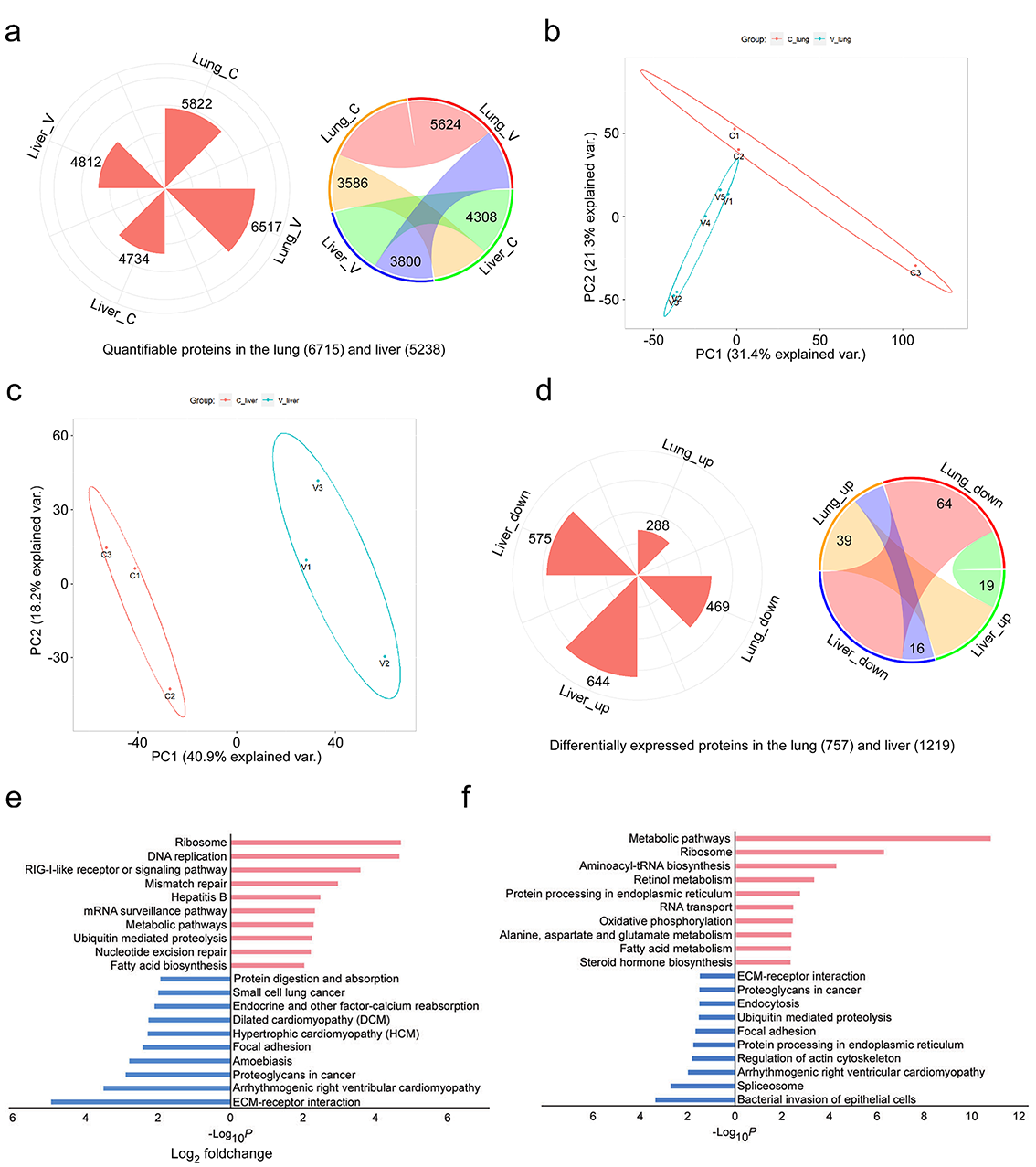
3.差异蛋白PPI互作分析
将通路富集到的蛋白进行蛋白相互作用(PPI)分析。肺部(图3a)和肝脏(图3b)在感染后均出现代谢相关蛋白和核糖体相关蛋白水平升高。结合KEGG和STRING数据库,发现感染组肺组织RIG-I通路、蛋白加工、DNA复制和修复相关蛋白上调,肝组织氧化呼吸链和蛋白质加工通路相关蛋白发生显著变化。蛋白酶介导的蛋白质降解在肺中活跃,但在肝脏中受到抑制(图3c,d)。同时发现,SARS-CoV-2感染7天后,局灶性粘连周围蛋白呈下降趋势。整合素α家族中的ITGA5和链接ECM和细胞骨架的DAG1在感染肺和肝脏组织中均下降(图3c,d)。
磷酸化是细胞对刺激做出反应的一种快速调节方法,已在一些SARS-CoV-2感染的细胞模型或尸检样本中检测到。因此,作者分析了恒河猴肺和肝脏的磷酸化蛋白质组,以期找到SARS-CoV-2感染期间的潜在药物靶点。共定量了肺中4185个蛋白质的12,418个磷酸位点和肝脏中3191个蛋白质的8134个磷酸化位点。其中,肺部873个蛋白质的1162个位点和肝脏712个蛋白质中的960个位点差异表达。通路富集和PPI互作分析发现,肺中上调的磷酸化蛋白富集于代谢、剪接体和泛素介导的蛋白水解等途径,而下调磷酸化蛋白与Fc-γ-R介导的吞噬、粘附连接和基础转录因子相关(图4a)。在肝脏中,上调的磷酸化蛋白富集于多种代谢途径,而下调的磷酸化蛋白与基础转录因子、剪接体、RNA转运等相关(图4b)。PPI互作结果显示,上调的磷酸化蛋白多于下调的磷酸化蛋白(图4c,d)。

图4 恒河猴肺、肝中差异磷酸化蛋白KEGG通路富集和PPI分析
5. 恒河猴SARS-CoV-2感染后肺、肝组织激酶预测
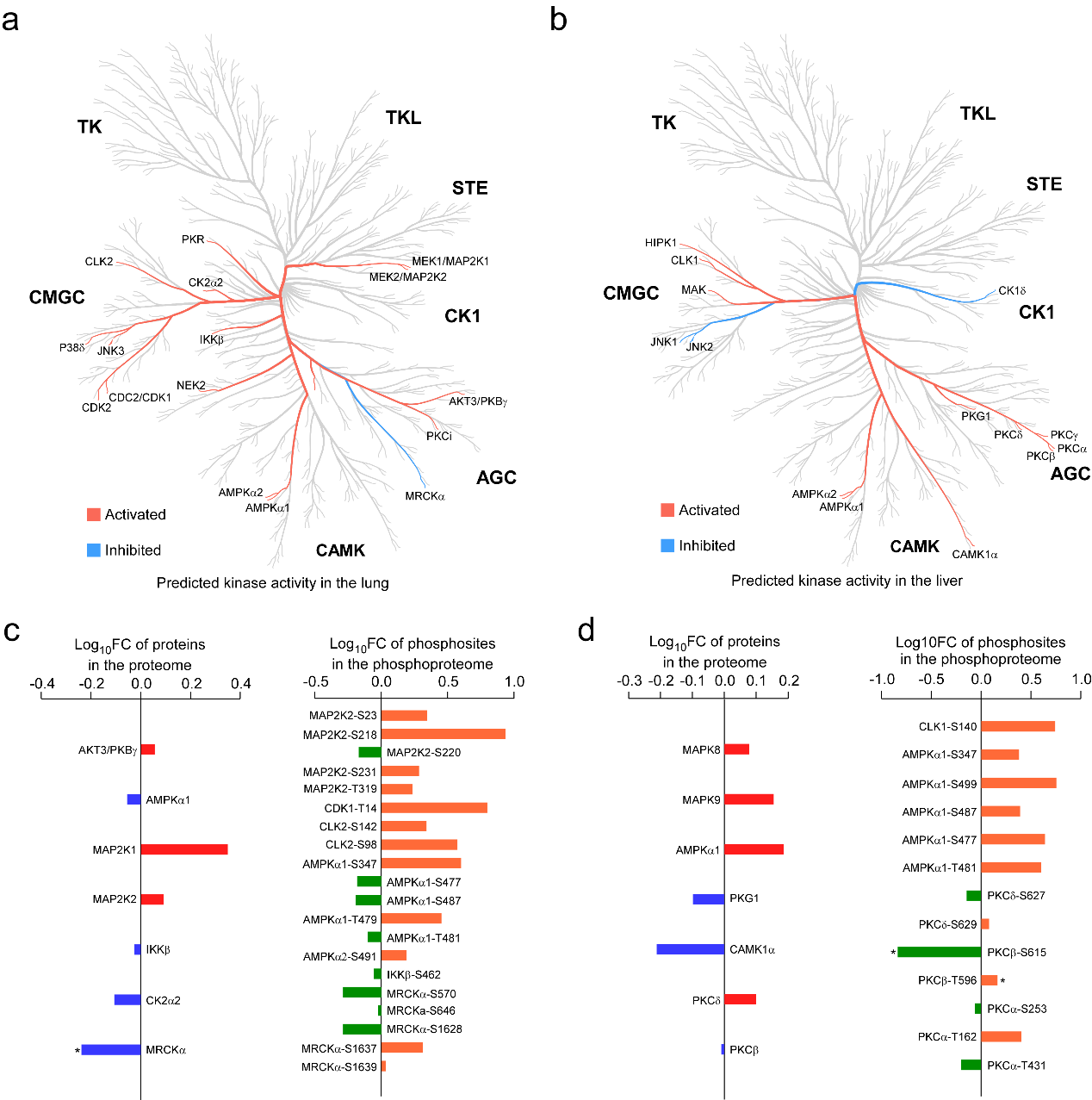
图5 恒河猴肺和肝中的激酶分析
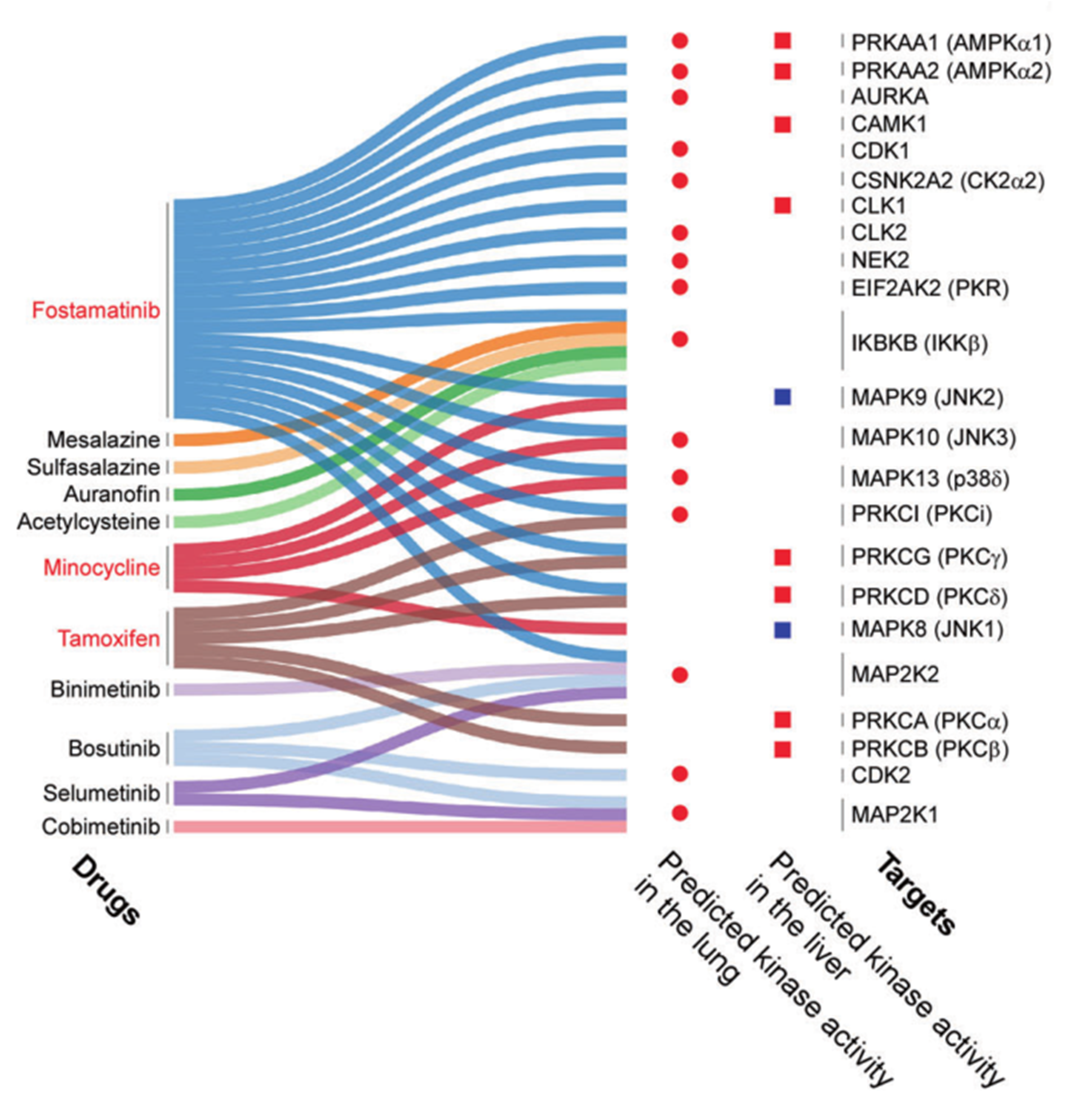
图6 药物与恒河猴肺和肝中的激酶桑基图
小结:
