大家好,这里是只想咕咕的椰球。今天为大家带来一篇轻松有趣的论文,标题为生酮饮食在阿尔茨海默小鼠模型中缓解认知损伤并减轻炎症反应。本文刊载于Wiley旗下的杂志CNS neuroscience & therapeutic。自2008年创立以来,这本刊物的影响因子一直不温不火地徘徊在3-4的区间。但是从18-19年开始本刊发展势头迅猛,影响因子一路上涨,截至今年已经突破7。本文的第一作者许云龙博士和通讯作者朱英杰研究员均来自中科院深圳先进技术研究院。

引言
“生酮饮食”是近几年非常受关注的一种膳食减肥策略,指的是一种严格的低碳水,高脂肪饮食方式。所谓“生酮”指的就是产生酮体(以丙酮酸和β-羟基丁酸为主),用脂肪代谢产生的酮体而不是葡萄糖为身体供能。自上世纪20年代被引入,生酮饮食已经被证明是一种有效的应对儿童难治性癫痫的疗法。目前生酮饮食治疗癫痫的原理尚未明确,不过科学家普遍认为生酮饮食可以增加体内γ-氨基丁酸(GABA)水平从而降低神经元兴奋度,同时还具备调节肠道菌群的作用。除此之外其他研究也表明,生酮饮食可以起到抗炎、抗氧化等神经保护作用,这提示生酮饮食除了可以治疗癫痫,还有可能对其他神经退行性疾病产生保护和治疗作用。
阿尔茨海默病(Alzheimer's disease,AD)是世界第一大神经退行性疾病,威胁着数千万老龄人群的身体健康和生活质量。AD的发病机理仍未完全清楚,但是普遍认为和神经炎症存在千丝万缕的联系。因此生酮饮食作为治疗阿尔茨海默病的疗法,其潜力值得探索。
在本文中,研究者探讨了生酮饮食对阿尔茨海默模型小鼠的治疗作用。利用5xFAD模型鼠以及多种行为学、组织学手段,作者发现生酮饮食干预可以显著减轻AD模型鼠的神经炎症,阻止AD模型鼠神经元和突触的丢失从而减轻AD模型鼠的认知功能损伤。
结果
为了在模式动物中模拟阿尔茨海默病的病理特征,多种AD动物模型已经被开发出来。目前最广泛被使用AD动物模型是转基因小鼠模型。如APP/PS1、3xTG等携带AD致病突变体的转基因小鼠模型都已经为人熟知了。在本研究中作者使用的5xFAD鼠携带了5种人源的家族性AD相关突变基因,属于AD疾病进展最快的转基因鼠模型之一。在本文的研究中,模型动物和对照动物被分为3组,分别为AD+KD(模型鼠+生酮饮食)、AD+SD(模型鼠+标准饮食)和WT+SD(野生型鼠+标准饮食),是一个比较标准的实验组+阳性对照+阴性对照的分组设计。饮食干预从动物7月龄时开始,此时5xFAD鼠已经表现出了严重的AD表型(图 1A)。在连续四个月对模型鼠进行生酮饮食干预后,研究者使用不同的行为学范式对各组动物的学习记忆和运动能力进行了测试。
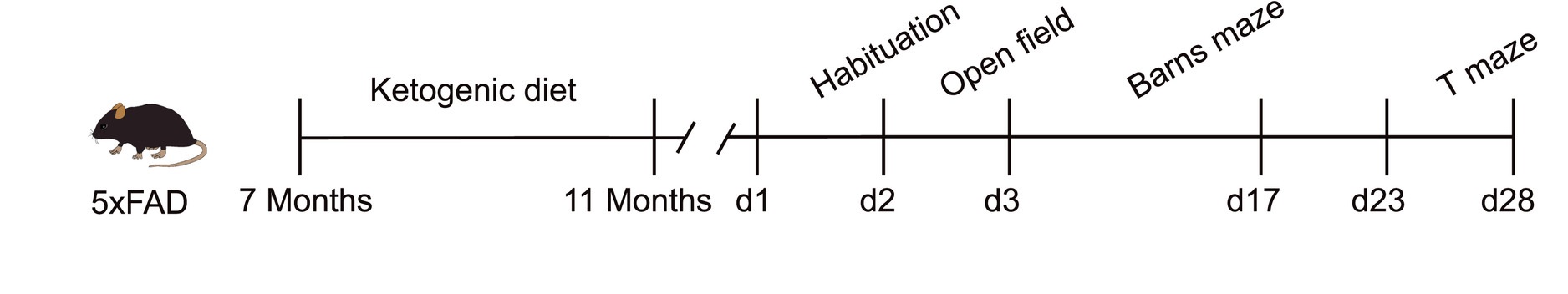
图1 本文实验流程图,包含饮食干预和行为测试
首先,作者使用旷场实验(open filed test,OFT)检验了各组小鼠的运动能力和焦虑水平。结果表明三组动物在旷场中的平均运动速度和总运动距离未表现出显著差别(图 2A和B),这提示动物的运动能力和运动意愿均未因品系和饮食干预而发生显著改变。同时三组动物在旷场中心活动的时间和进入旷场中心的次数也未表现出显著区别,这表明不同品系动物或不同饮食干预均未对动物的焦虑水平产生显著影响。
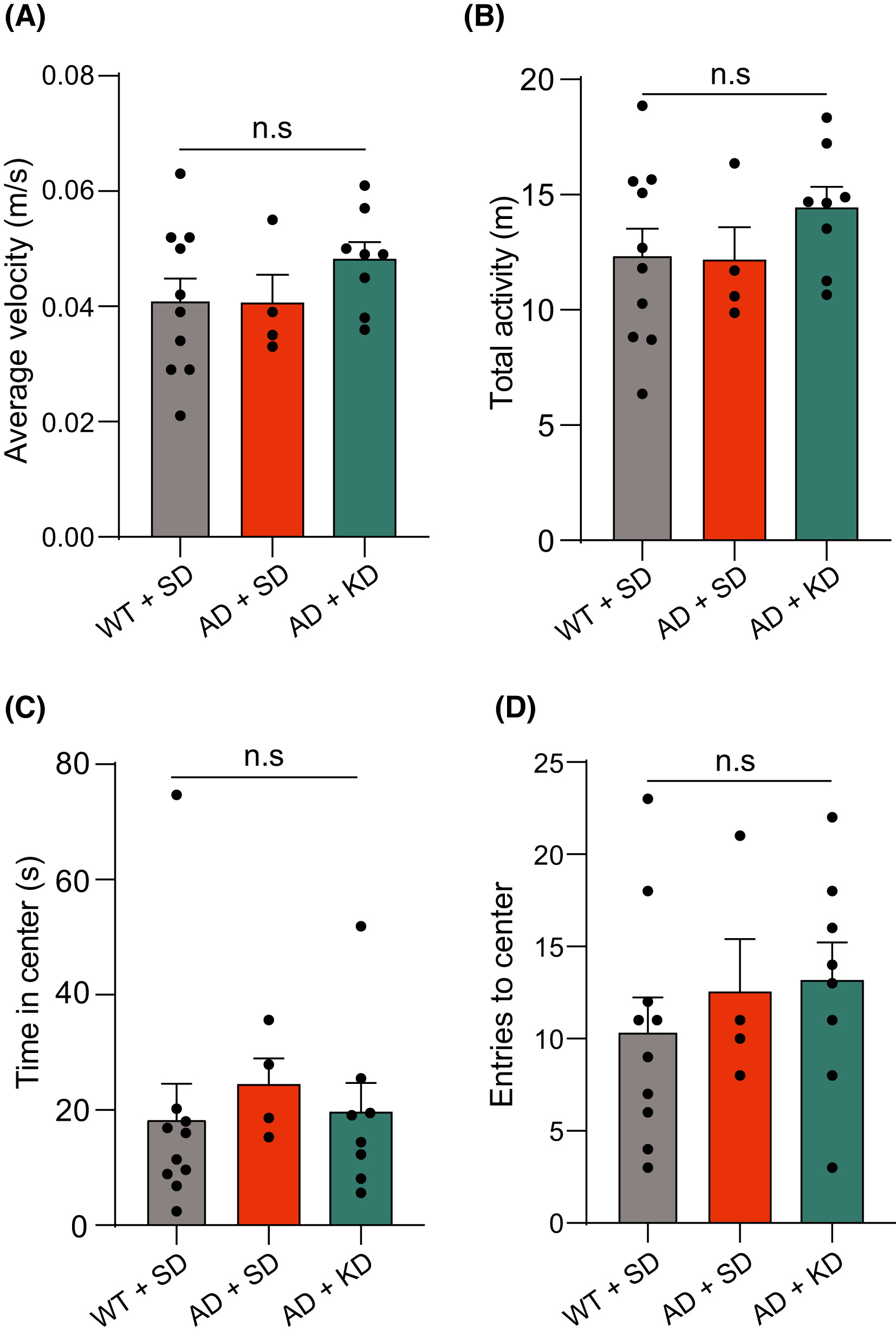
图2 旷场实验检测不同饮食干预的AD模型鼠和野生鼠的运动能力和焦虑水平
在确认动物的运动和情绪水平未受改变后,研究者对动物的学习记忆能力进行了检验。
当研究动物学习记忆能力时我们通常会设置“一长一短”两种行为范式。具体而言,我们分别需要分别设置一个长期记忆(参考记忆)科目和一个短期记忆(工作记忆)科目,通过两种行为学实验的结果交叉验证从而阐明不同组别动物之间学习记忆能力的差别。
在本研究中,作者使用Barnes迷宫对动物的空间学习记忆能力进行测试(图 3B)。Barnes迷宫可以被看为是Morris水迷宫的陆地版,相比水迷宫实验,Barnes迷宫对动物的体能消耗更小,动物的应激水平也更低。另外,研究者选用T迷宫作为工作记忆的范式(图 3F)。T迷宫,或者与其相似的Y迷宫都是检验动物工作记忆的常用范式。研究者在本文设计了一个“延迟非配对”任务训练动物在两次连续的试验中分别向迷宫的两臂移动。
Barnes迷宫的结果表明,经过8天的训练后,野生型鼠和以生酮饮食喂养的AD模型鼠的平均逃避潜伏期均降至50s以内,而正常饮食的AD模型鼠逃避潜伏期依然保持在100s以上(图 3C)。在空间探索测试中,AD模型鼠首次进入藏身洞的时间显著长于野生鼠,在目标象限探索的时间比例也显著短于野生鼠(图 3D和3E)。然而,使用生酮饮食干预则使得AD模型鼠在Barnes迷宫的两个评价指标中均优于普通饮食组模型鼠。
同时,T迷宫实验的结果与Barnes迷宫的结果相吻合。普通饮食处理的AD模型鼠在任务正确率上显著低于野生型对照鼠,而生酮饮食组AD模型鼠在T迷宫中的任务正确率则相比普通饮食组存在显著的提升(图 3G)。
综上,在AD模型鼠发病之后采取生酮饮食干预使得模型鼠的认知障碍症状得到了显著的缓解,提示生酮饮食治疗AD导致认知损伤治疗方案的潜力。

图3 生酮饮食可以缓解5xFAD模型鼠的认知功能损伤
除了认知障碍外,皮层和海马区神经元的丢失和突触的损伤也是AD的典型症状。因此研究者接下来在检验了生酮饮食干预对神经元和突触的保护效果。首先,作者分别使用突触素(Synaptophysin)和PSD95两种抗体对海马齿状回组织的切片进行免疫荧光染色。突触素是突触前小泡的标志蛋白,而PSD95是突触后致密带蛋白,两种抗体分别代表了突触的两个组成部分。结果显示,无论是突触素还是PSD95,在AD模型鼠中量的相比野生鼠均显示出显著的下降,表明随着AD病程的进展所表现出的突触缺失(图 4A和C)。而在生酮饮食干预的AD模型鼠中两种标志蛋白的斑块数量相比普通饮食的模型鼠均表现出一定的回升(图 4B和D),提示生酮饮食干预可以部分阻止5xFAD鼠中突触的损伤。
同时,使用成熟神经元标志物NeuN免疫荧光染色,研究者还检验了生酮饮食对AD模型鼠中神经元丢失的保护作用。结果显示,11月龄的5xFAD鼠中发生了神经元大量缺失的现象,而生酮饮食则在一定程度上抑制了NeuN阳性细胞丢失的现象(图 4E-H)。
为了判定突触的缺失原发还是是由神经元死亡所导致的,研究者使用高尔基银染的办法对皮层和海马区幸存神经元树突的形态进行了观察(图 4I)。结果表明AD模型鼠中单位长度树突棘的密度显著低于野生鼠,而在生酮饮食处理的AD模型鼠中树突棘的密度则得到了有效的恢复(图 4J)。以上结果进一步证明生酮饮食可以在一定程度上阻止AD模型鼠中突触和神经元的损伤。

图4 生酮饮食阻止了AD模型鼠中神经元和突触的丢失
除了细胞丢失和认知障碍外,AD的典型病理特征还包括β-淀粉样蛋白(β amyloid,Aβ)的沉积、tau蛋白的缠结以及小胶质细胞的激活等。因此在接下来的研究中,作者对这几项指标进行了检测。免疫荧光结果表明,普通饮食组AD模型鼠中出现了大量Aβ斑块积累,而生酮饮食处理的AD模型鼠中Aβ斑块的面积则显著更小(图 5A和B)。小胶质细胞标志物Iba-1染色的结果表明AD模型鼠中小胶质细胞的激活水平显著高于野生鼠,形态也显著膨大(图5C和E);而生酮饮食处理的AD模型鼠中小胶质细胞的激活水平和形态则与野生鼠相当(图 5C和D)。同时,研究者还检查了脑组织中部分炎性因子的表达水平,ELISA结果显示在皮层和海马两个脑区中,生酮饮食干预均可以显著减轻AD模型引发的IL-1β和TNF-α表达量的上升(图 5G-5J)。
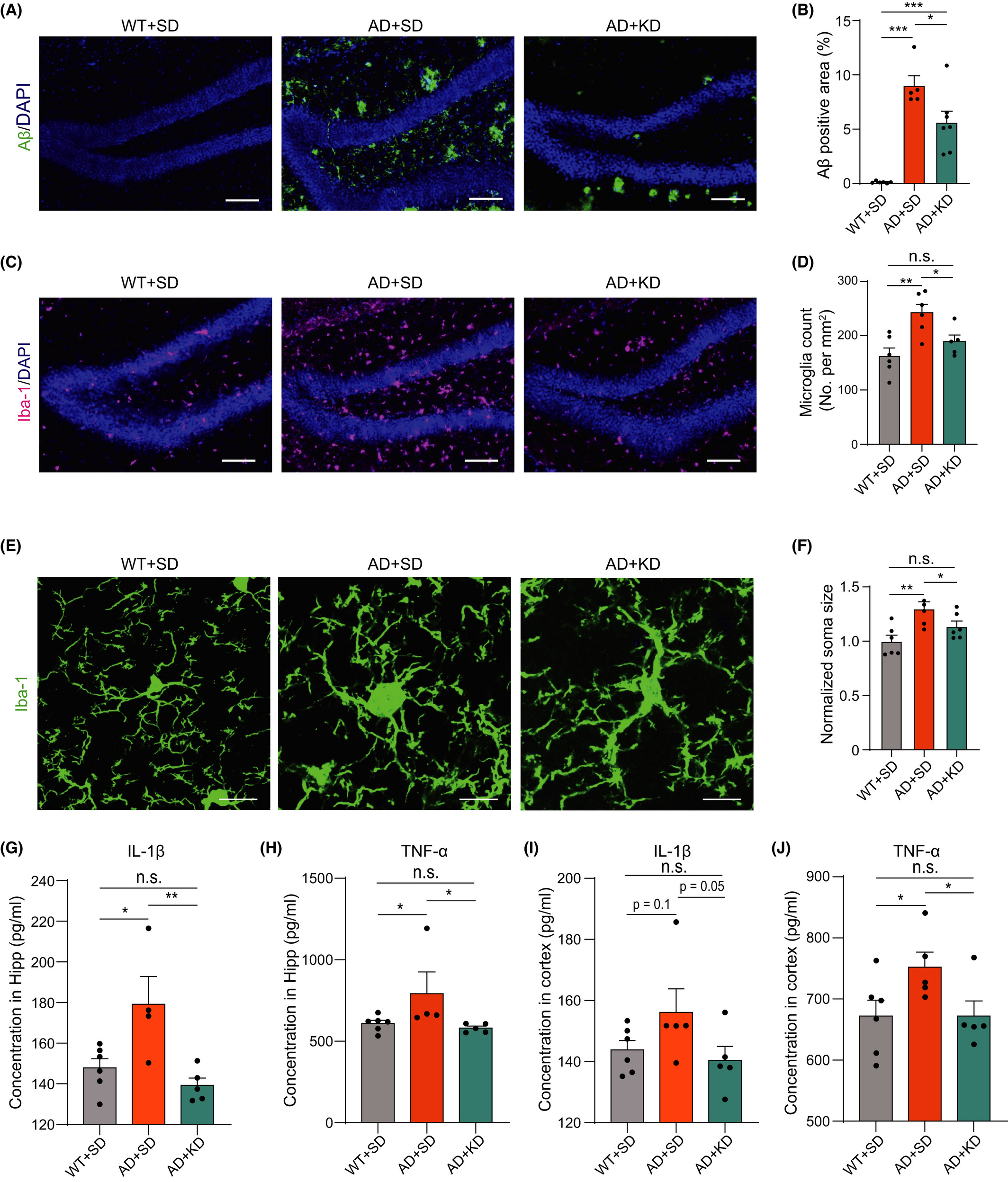
图5 生酮饮食可以减轻5xFAD小鼠中 Aβ的沉积和小胶质细胞的活化
综上,本文使用阿尔茨海默模型小鼠,通过多种行为学和病理手段检测了生酮饮食法对阿尔茨海默模型小鼠的治疗作用。本文的研究内容并不复杂,但是研究和行文的思路清晰,所采用的研究方法全面包含了阿尔茨海默药效研究的各个方面。我们将本文中所采用的动物模型和研究方法整理在下表中,希望对有AD相关疗法评筛需求的朋友们有所帮助。
| 研究内容 | 本文采用了 | 还可以采用 |
| AD模型动物 | 5xFAD转基因模型鼠 | APP/PS1模型鼠、3xTG模型鼠 |
| 空间学习记忆 | Barnes迷宫 | Morris水迷宫 |
| 工作记忆/短期记忆 | T迷宫 | Y迷宫,新物体识别 |
| 神经元、突触丢失 | 突触素/PSD95染色; NeuN染色、高尔基染色 | vGLUT2染色、尼氏染色 |
| Aβ、tau斑块沉积 | Aβ1-42染色 | tau染色, 硫磺素T染色 |
| 小胶质细胞激活 | Iba-1染色 | Cd11染色 |
| 神经炎性反应 | ELISA检测炎性因子 | WB、qPCR检测炎症相关因子 |
| 突触可塑性 |
- |
膜片钳电生理检测LTP |
